第17回iPERCセミナーを開催しました
- 2024/09/06
2024年2月27日、静岡大学光創起イノベーション研究拠点棟にて、Robert Virgil Warren先生によるJournal Clubが開催されました。Warren先生はバイオメディカルの専門家であり、浜松ホトニクス株式会社の米国法人に所属されています。
このJournal Clubでは、静岡大学と浜松医科大学の学生がWarren先生の指導のもとで一つの英語の学術論文を選び、役割を分担して発表しました。発表会では、Warren先生や参加者が発表内容について議論しました。Warren先生は静岡大学浜松キャンパスに来訪され、会場でのリアル開催とZoomを併用したハイブリッド形式でした。発表者は浜松医科大学医学部医学科5年の小原弘大さん、4年の友近祐奈さん、静岡大学の創造科学技術大学院情報科学専攻博士課程2年の吉野朱香さん、ナノビジョン工学専攻博士課程2年のKwen Hyeun Wooさんでした。
今回は、アメリカ合衆国ライス大学のJ.B. Cooleらによる「Multimodal optical imaging with real-time projection of cancer risk and biopsy guidance maps for early oral cancer diagnosis and treatment」[1]を題材に議論が行われました。この論文は、口腔がんの早期発見と治療を支援するためのポータブルで低コストなアクティブバイオプシー(注1)ガイダンスシステム(ABGS)を提案しています。ABGSは、広視野自家蛍光(注2)画像と高解像度顕微鏡画像を深層学習(注3)により解析してがんリスクマップを作成し、それを生検ガイダンスマップとしてリアルタイムで生体組織上に直接投影することで、早期病変部位の特定と適切な生検部位の選択を支援することが期待されています。
発表概要
浜松医科大学 友近 祐奈さん
口腔がんの症状、リスク要因、診断方法、および従来の手法の問題点と早期発見の重要性について説明されました。口腔がんの多くは、がん発症に先行して、症状からわかる口腔潜在性悪性疾患(OPMD、注4)や顕微鏡観察で見つけられる口腔上皮異形成(OED、注5)が認められます。OEDの診断は口腔病変の生検により行われますが、経験豊富な臨床医でさえ、いつ、そして患部のどこを生検(注1)するかを決めるのは困難です。それを改善するためのABGSについて説明がありました。ABGSが広視野自家蛍光イメージング、高解像度顕微鏡イメージングによるがんリスクと生検ガイダンスマップを提供することで、口腔がんおよびその前がん病変の早期発見に役立つ可能性について説明されました。
静岡大学 Kwen Hyeun Wooさん
ABGSの構成、原理とそのワークフローについて説明されました。広視野自家蛍光画像と高解像度顕微鏡画像を取得し、深層学習を利用したプログラムでがんリスクを統合解析して、最終的に生検ガイダンスマップとして患者の口腔内にプロジェクタで投影されます。最後に、カメラとプロジェクタの空間解像度とミスアライメントの評価についても説明がありました。
浜松医科大学 小原 弘大さん
論文で示されたABGSシステムを実際の患者3名に適用した結果が説明されました。患者1については右側舌の病変部位にてABGSの全ワークフローが行われました。患者1の顕微鏡画像は、高解像度モザイク解析で評価され、高リスク領域のMTNスコア(注6)は低リスク領域より高く、核が密集・拡大する傾向がありました。医師は臨床的に疑わしい領域から3カ所(2カ所は高リスク領域、1カ所は低リスク領域)の生検を実施し、病理検査で中等度から高度の異形成(注7)が確認されました。一方で、患者2では広視野白色光と自家蛍光イメージングによるがんリスクマップを作成し、口腔粘膜に投影して高リスク領域を特定しました。最後に、患者3では、広視野白色光と自家蛍光イメージングによるがんリスクマップを口腔粘膜に投影し、高リスク領域から顕微鏡画像を取得しました。マルチモーダル画像診断が行われた後、がんリスクマップに基づいて外科的切除が行われ、病理組織学的解析の結果、中等度分化の浸潤性扁平上皮癌(注8)が確認されました。
静岡大学 吉野 朱香さん
論文のDiscussionの内容について説明がありました。提案システムはマルチモーダル画像診断によるがんリスクマップと生検ガイダンスマップを直接患者の組織にリアルタイムで投影し、高リスク領域の生検をガイドします。本システムの利点は、診断マップを対象領域に投影することで、ヒューマンエラーを減らし、臨床医がより正確に作業できるようにする点です。さらに、低コスト、容易な拡張性、多用途性が挙げられました。次に、本研究における診断スコアリングについて説明がありました。本研究で使用されたMTNスコアは、核およびケラチンのセグメンテーションと内部品質チェックを組み合わせることで、以前のアルゴリズムよりも優れた性能を示しました。次に、本システムのさらなる向上のために、高フレームレート(注 9)顕微鏡を用いて測定範囲を拡大し、システムの診断能力を上げる必要性が指摘されました。リアルタイムで実行可能な視覚ガイダンスを提供することで、臨床医が高リスク領域を正確に特定し、生検をガイドするのに役立ちます。最後に、このシステムが診断精度と患者ケアの向上に大きく貢献する可能性について説明しました。
論文の概要
口腔がんは世界的に重要な健康問題であり、その早期診断は治療関連死(注10)を減少させ、長期生存率を向上させる上で重要な役割を果たしています。口腔がんの病変は生検によって診断されますが、経験豊富な臨床医でさえ、どのタイミングで組織のどの部位の生検を行うかを選択するのは困難です。著者らは、口腔がんの早期発見をサポートするアクティブバイオプシーガイダンスシステム(ABGS)を提案しました。ABGSは、マルチモーダル光学イメージングと深層学習アルゴリズムを融合させ、がんリスクマップと生検ガイダンスマップをリアルタイムで患者に直接投影します。これにより、臨床医は高リスク領域を迅速に特定し、適切な生検部位を選択できるようになります。この革新的なシステムは、口腔がんの早期発見に貢献し、患者の転帰(注 11)の改善と生存率の向上を目的としています。
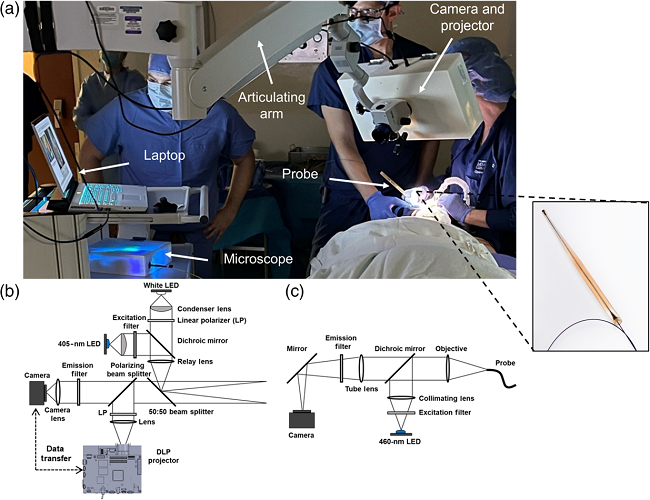
ABGSは図1に示す通り、広視野白色光および自家蛍光イメージングのためのカメラ、がんリスクマップの投影のためのプロジェクタ、光ファイバープローブを備えた顕微鏡から構成されています。このシステムは、口腔がんおよびその前がん病変の早期発見を目指して、臨床医が生検の必要性を判断するための広視野自家蛍光イメージングおよび顕微鏡イメージングを活用する手技をガイドします。
図1 ABGSの光学システムと臨床実装:(a)手術室で使用中のABGS、挿入図は顕微鏡イメージングプローブの拡大図を示しています、(b)ABGSカメラとプロジェクタの光学図、(c)ABGS顕微鏡の光学図。
LED:発光ダイオード(Light Emitting Diode)、DLP:デジタル光処理(Digital Light Processing)。
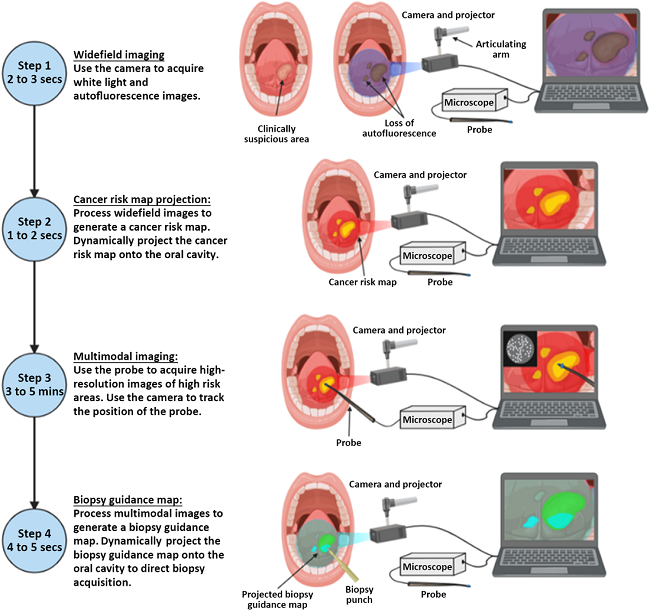
図2に示すABGSのワークフローでは、広視野自家蛍光イメージング、がんリスクマップの作成、顕微鏡画像の取得とプローブ位置の追跡、生検ガイダンスマップの口腔への投影といったステップを行います。深層学習アルゴリズムと広視野自家蛍光イメージングより、がんリスクマップが生成され、マルチモーダルイメージングの統合により、口腔がんおよびその前がん病変の早期発見が促進され、最終的に患者の転帰が改善されます。
図2 ABGSの撮像ワークフロー。(ステップ1:カメラとプロジェクタを用いて広視野画像を取得する。ステップ2:がんリスクマップを作成し、口腔内に投影される。ステップ3: 高リスク領域から顕微鏡画像を取得する。ステップ4:マルチモーダル画像データを処理して生検ガイダンスマップを作成し、口腔内に投影する)。
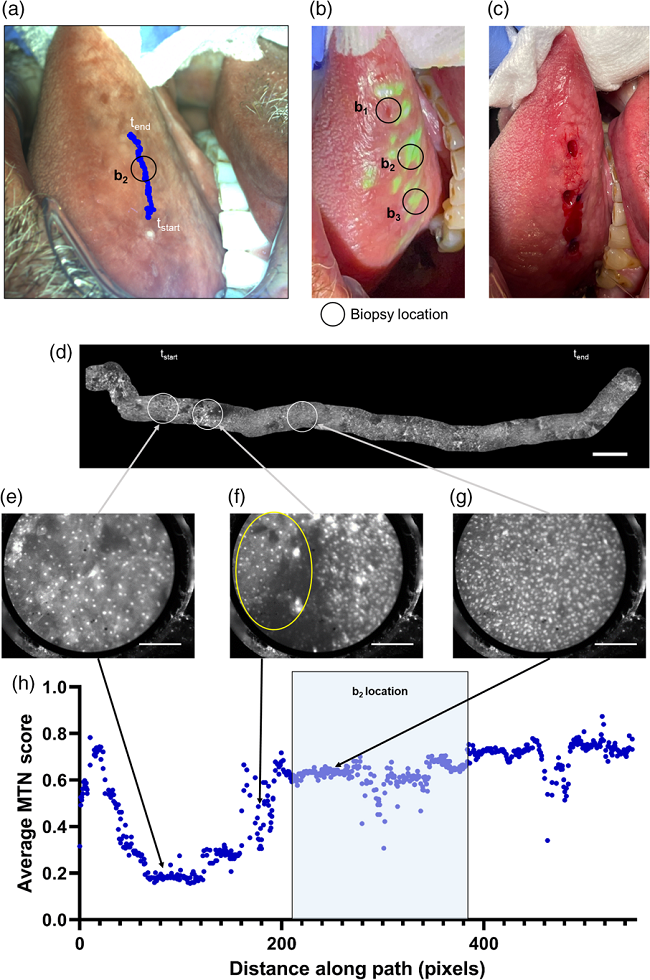
図3はABGSによる右側舌の病変の診断結果です。生検は臨床的に疑わしい領域と生検ガイダンスマップで強調された領域の両方で行いました(図3(b)~(c))。顕微鏡画像は分析され、幅16.3 mmの高解像度モザイクが生成されました(図3(d))。顕微鏡画像の各ピクセルで平均MTNスコアを計算しました。図3(e)~(g)に示されるのは、低リスク領域は正常な核を持つ顕微鏡画像、正常な核から密集・拡大した核の領域の間の遷移領域を示す顕微鏡画像、そして高リスク領域からは密集して拡大した核を持つ顕微鏡画像です。高MTNスコアを持つ領域は、臨床的に疑わしい領域および生検ガイダンスマップで強調された領域に対応しており、病理組織学的解析では中等度から重度の異形成が確認されました。
結論として、がんリスクと生検ガイダンスマップをリアルタイムで患者に投影するアクティブ生検ガイダンスシステムの有効性が実証され、生検部位の選択精度の向上が期待されます。
図3右側舌の病変におけるマルチモーダルイメージングの解析、(a)臨床的に疑わしい部位のWL画像、(b)生検ガイダンスマップを口腔内に投影したWL画像、(c)マルチモーダルイメージング後に採取された生検の画像、(d)マルチモーダルイメージングデータから生成された高解像度モザイク画像。(e)正常な核を示す顕微鏡画像。(f)正常な核の領域(黄色の楕円)と、核が密集・拡大した領域の間の遷移領域を示す顕微鏡画像。(g) 密集・拡大した核を示す顕微鏡画像。(h)顕微鏡画像から得られた平均MTN診断スコアと撮影経路上の距離との関係
質疑応答集
Q1:口腔がんの早期発見のために、口腔に軽い症状が何日続いたら、医師の診察を受ける方がいいですか?
発表者: 「定期的な健康診断を受けている患者の場合、その患者を日頃診ている歯科医が、患者本人よりも早く口内の病変を見つけることができる場合があります。」
Warren先生: 「一般的には、症状が3週間以上続く場合は医療機関を受診することが勧められます。今回紹介するABGSなどの高度な診断技術を用いられるようになれば早期に発見されるようになるかもしれません。」
Q2:イメージングのステップ3について質問があります。3分から5分かかるとありましたが、その間ずっと舌を動かさないでいるのは大変ではありませんか?
発表者: 「はい、舌を3分から5分間動かさないのは大変だと思います。この間プローブがこのエリア全体を検出するので、舌を動かさないようにする必要があります。」
Warren先生: 「もし患者が舌を動かした場合、ステップ1と2では問題ないと思いますが、ステップ3や4では実験を最初からやり直す必要があるかもしれません。動きに対する補正を行うことは可能かもしれませんが、この研究では行われていないと思います。」
Q3:口腔癌は舌だけに限定されるのですか?それとも口全体に発生するのですか?
発表者: 「口腔がんは舌だけでなく、口全体に発生する可能性があります。異なる部位にがんがある場合、より複雑なスキャンが必要です。」
Q4:例えば乳癌の場合、自分で触診して良性か悪性かを判断できますが、口腔癌の場合はどうでしょうか?
Warren先生: 「口腔がんは乳がんと比べて判断が難しいかもしれませんが、何か異常が2週間以上続く場合は医師に診てもらうことをお勧めします。」
Q5:正常組織と癌組織をどのように区別しますか?
発表者: 「がん組織では、正常組織に比べて自家蛍光が減弱していることがあります。これが腫瘍の兆候です。また、ポルフィリンの量も重要です。正常組織と比べて、がん組織ではリンパ系が欠如していて、そのためにポルフィリンを排出できず、結果としてポルフィリンの強度が高いです。」
Warren先生: 「また、コラーゲンの信号も変化します。ポルフィリン信号とコラーゲン信号の比率を使って、正常組織とがん組織を区別できます。」
Q6:この技術で使用される顕微鏡の観察可能深度はどの程度ですか?
発表者: 「使用される共焦点顕微鏡は比較的表面的な観察に適しており、深部までは見えません。」
Q7:なぜ多くの顕微鏡画像が必要なのですか?
発表者: 「多くの顕微鏡画像が必要なのは、各ポイントでの画像のヒントを比較するためです。高フレームレートでの撮影により、複数の画像を使用することで、結果の品質が向上します。」
Warren先生: 「この研究では、データのサンプリング密度が高すぎる可能性があり、もっと低密度にしても問題ないかもしれません。より高速で顕微鏡ファイバープローブを動かしても、おそらく大丈夫だと思います(30秒から1分程度)。プローブを大きくすることも検討できると思います。」
Q8: がんを検出するためのアルゴリズムはどのように開発されましたか?
Warren先生: 「彼らは以前の研究で、がん、重度異形成など様々なタイプのがん細胞を用いてアルゴリズムを訓練しました。今回発表された研究では、3人の患者全員に対して生体検査を行い、アルゴリズムによる診断結果と照合したところ、かなり良好な一致が見られたそうです。しかし、3人という少人数での検証では十分とは言えません。より多くの患者で検証を行い、信頼性を高める必要があります。」
Q9: この研究で最も印象に残った点、またはよくできていたと思う点は?(Warren先生から)
発表者: 「パフォーマンス向上のためには、品質チェック機能の導入が重要だと感じました。短時間の露光時間で観察できた点、患者さんがじっとしていられた点が最も印象に残りました。」
Q10: この研究を改善するにはどうすれば良いか?(Warren先生から)
発表者: 「初めに大きいプローブで検査を行い、疑わしい部分が見つかったら小さいプローブに切り替えることができます。」
参加者: 「スマートフォンカメラで検出できるようにし、AR/VR技術を活用することもできます。」
報告者の感想
今回の論文は、広視野自家蛍光イメージング、高解像度顕微鏡イメージング(工学・医学)と深層学習(情報学)を融合した点で、非常にジャーナルクラブに適した内容でした。ABGS装置を用いて、口腔がんの生検部位の選択をサポートし、がんの早期検出と早期診断に役立つことが感心しました。筆者自身の研究テーマは火傷や糖尿病足病変の早期診断を目指すCMOSイメージセンサを用いた定量生体計測であり、本研究は筆者にとって非常に関心のある分野でした。今回、ジャーナルクラブを通して学生や先生を問わず活発に論文について議論がなされました。工学、医学、情報学の融合的な場面で議論できたことは、非常に良い機会となりました。最後に、ジャーナルクラブの指導をしてくださったWarren先生、発表資料を用意してくださった学生さん、そして静岡大学・浜松医科大学の関係者の方々に感謝いたします。
引用文献
[1] J. B. Coole et al., “Multimodal optical imaging with real-time projection of cancer risk and biopsy guidance maps for early oral cancer diagnosis and treatment,” J Biomed Opt., 28(1), 016002 (2023).
(注1) バイオプシー(biopsy): 生体組織採取検査、あるいは生体組織診断(通常、生検と略称)。診断のために身体の組織の一部を採取して、顕微鏡等を用いて病理組織学的に検査することです。
(注2) 自家蛍光(autofluorescence):タンパク質、核酸、低分子化合物等、生体を構成する化学物質が発する蛍光(照射した光を吸収して放出する(通常は照射光より長波長の光))。これは、人工的に加えられた蛍光マーカーの蛍光とは異なります。
(注3) 深層学習(ディープラーニング): 人間の神経細胞の仕組みを再現したニューラルネットワークを用いた機械学習の手法の1つであり、多層構造のニューラルネットワークを用いることが特徴です。
(注4) 口腔潜在性悪性疾患(OPMD: Oral Potentially Malignant Disorders): 口腔潜在的悪性病変(前がん病変)は,現在障害は起こしていないが明らかに異常な状態にあり,悪性を強く疑わせる病変.
(注5) 口腔上皮性異形成(OED: Oral epithelial dysplasia):遺伝子変化の蓄積によって上皮の構造異型や細胞異型を示し,扁平上皮癌に進行するリスクが高い病変.
(注6) MTNスコア: 本研究では、がん診断のためのマルチモーダル光学イメージングにおいて、マルチタスク深層学習ネットワーク(MTN: multitask deep learning network)によって生成される診断スコアを指します。MTNスコアは、顕微鏡画像フレームごとに計算され、核形態や組織構造などの画像で観察された特徴に基づいて、異常な細胞形態の可能性を評価するために使用される。
(注7) 異形成:細胞が分裂して分化して臓器が作られる過程で異常が生じ、臓器が正常に形成できない状態を指します。
(注8) 浸潤性扁平上皮癌:上皮細胞から発生したがんが基底膜を破って間質に浸潤する段階のがんです。
(注 9) フレームレート: 1秒間に撮影される画像の数を示す重要な指標です。フレームレートの高い顕微鏡を使用することで、一つの部位の測定にかかる時間を短縮し、測定範囲を広げることができます。
(注 10) 治療関連死(treatment-related morbidity) 本来の意味は「医療機関での治療中におきた死」であり、通常の病死と区別するための言葉ですが、この論文での筆者の意図は、「治療を始めてからの死亡」という意味で使っていると思われます。早期発見でない場合、がんのステージが進んでしまっていることも多いので、治療(手術等)の侵襲がより大きくなることも大いに考えられ、本来の意味での治療関連死も増える可能性はあるとは考えられます。
(注 11) 転帰:病気の進行と治療の結果、患者が至る状態を指します。具体的には、病気や症状がどのような最終的な結果に至るか、例えば回復、悪化、慢性化、または死亡などの状態を意味します。
- 2025/01/21
- 第18回iPERCセミナーを開催しました
- 2024/09/06
- 第17回iPERCセミナーを開催しました
光創起イノベーション研究拠点棟 〈光創起研究棟〉
〒432-8011 静岡県浜松市中央区城北3丁目5-1 国立大学法人静岡大学浜松キャンパス内
TEL:053-478-3271 / FAX:053-478-3256